여기에 코로나19 대체 치료 의약품을 공급하는 회사도 15곳에 달해 코로나19 퇴치와 직·간접적으로 관련된 기업만 32개사에 이른다. 정부의 전폭적인 지원 대책까지 잇따르자, 팬데믹(Pandemic·세계적인 전염병 대유행) 상황에서 치료제·백신 개발에 성공할 경우 해외 각국의 긴급 승인 제도를 통한 수출길이 저절로 열리며 글로벌 제약사로 발돋움할 기회를 잡을 수 있을 것으로 보인다.
|
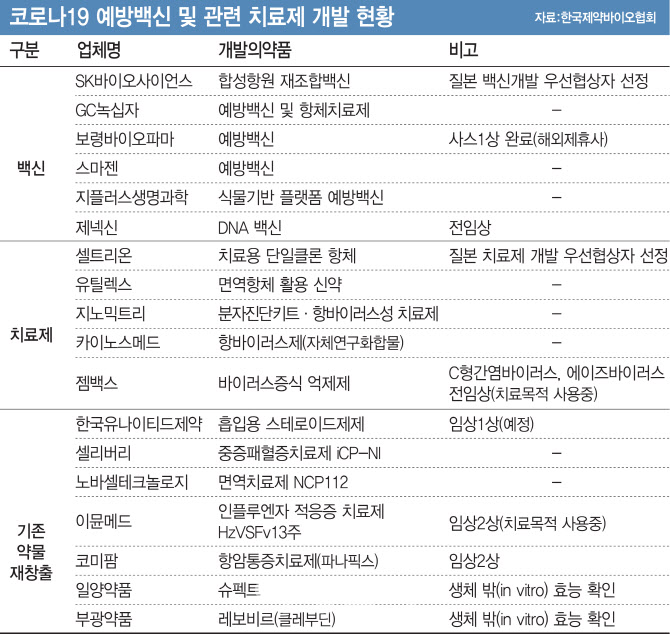
13일 제약·바이오업계에 따르면 코로나19 백신 개발업체는 SK바이오사이언스, GC녹십자(006280), 보령바이오파마, 스마젠, 지플러스생명과학, 제넥신(095700) 등 6곳이다. 치료제 개발업체는 셀트리온(068270), 유틸렉스(263050), 지노믹트리(228760), 카이노스메드, 젬백스(082270) 등 5곳에 달한다. 기존 약물 재창출에는 한국유나이티드제약, 셀리버리(268600), 노바셀테크놀로지, 이뮨메드, 코미팜(041960), 일양약품(007570), 부광약품(003000) 등 7곳이 뛰어들었다. 약물 재창출이란 이미 시판·사용되고 있어 안전성이 입증된 약물이나 임상시험에서 안전성은 있지만 효능이 충분히 입증되지 않아 허가 받지 못한 약물을 대상으로 새로운 적응증을 규명해 코로나19 신약으로 개발하는 방법이다.
|
현재 치료용 단일클론 항체 치료제 우선협상대상자인 셀트리온은 질병관리본부 신종감염병매개체연구과와 협업해 최종 항체 후보군을 확보했다. 두 차례에 걸쳐 중화능력 검증을 실시한 결과, 총 38개의 항체에서 중화능력을 확인했다. 이 중 14개의 항체는 강력한 중화능력을 보인 것으로 전해졌다. 이날부터 셀트리온은 최종 항체 후보군을 대상으로 세포주 개발에 착수했다.
유틸렉스는 면역항체를 활용한 신약 연구에 몰두하고 있다. 지노믹트리와 카이노스메드는 항바이러스 치료제를 개발하고 있는 것으로 알려졌다. 젬백스는 치료 목적으로 사용 중인 C형간염·에이즈 바이러스 전임상 약물을 코로나19 바이러스 증식 억제제로 쓸 수 있는지를 들여다보고 있다.
질본으로부터 백신개발 우선협상자에 선정된 SK바이오사이언스는 합성항원 재조합 백신을 만들고 있다. 녹십자는 예방 백신과 항체 치료제를 동시에 개발 중이다. 보령바이오파마는 해외 제휴사와 중증급성호흡기증후군(SARS·사스) 1상을 완료한 백신을 코로나19에도 적용할 수 있는지 연구 중이다. 스마젠은 예방 백신을, 지플러스생명과학은 식물기반 플랫폼 예방 백신을 각각 개발하고 있다. 제넥신은 DNA 백신을 개발 중인데 이르면 6월 중 인체 임상이 가능할 정도로 속도가 빠르다. 다음 달 초엔 동물 임상에 들어갈 것으로 보인다.
과학기술정보통신부·보건복지부·식품의약품안전처는 지난 9일 경기도 성남시 한국파스퇴르연구소에서 열린 코로나19 치료제·백신 개발 산업계·학계·연구소·병원 합동 회의에서 문재인 대통령에게 “다음 달 초에는 코로나19에 감염되는 영장류를 통해 치료제 1건, 백신 2건의 효능 검증에 돌입할 계획”이라고 밝혔다.
조만간 셀트리온이 치료제 및 백신 각 1건씩, 제넥신이 백신 1건에 관한 동물 임상 시험에 들어갈 것이란 관측이 나온다.
|
제넥신 속도 빨라…녹십자, 치료제·백신·대체의약품 모두 관여
앞서 문 대통령은 산·학·연·병 합동회의 자리에서 추가경정예산, 긴급연구자금, 예비비 등을 통해 △약물 재창출 △항체 치료제 △혈장 치료제 등 다양한 치료제 개발을 위한 긴급연구 지원을 약속했다. 특히 코로나19 백신 개발에 2100억원을 투자하겠다고 발표했다.
약물 재창출 연구·개발(R&D)에선 한국유나이티드제약의 흡입용 스테로이드제제가 임상 1상이 예정돼 있다. 셀리버리는 중증패혈증 치료제 ‘iCP-NI’에, 노바셀테크놀로지는 면역 치료제 ‘NCP112’에 대해 각각 코로나19 적응증 추가 여부를 살피고 있다. 이뮨메드는 인플루엔자 적응증 치료제 ‘HzVSF v13주’, 코미팜은 항암통증 치료제 ‘파나픽스’에 대한 임상 2상을 각각 진행하고 있다.
일양약품이 개발한 만성골수성 백혈병치료제인 슈펙트는 체외 시험관 내 시험(in vitro) 결과, 투여 후 48시간 내에 대조군 대비 코로나19 바이러스가 70% 가량 감소한 것으로 확인됐다. 부광약품의 항바이러스제 레보비르(클레부딘)는 에이즈 치료제이자 코로나 바이러스 치료제로 불리는 칼레트라와 유사한 결과를 보이고 있다.
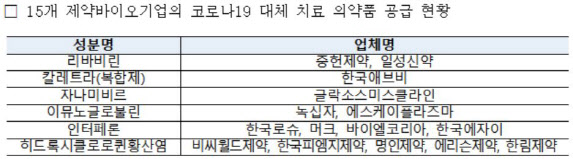
중헌제약, 일성신약(003120), 한국애브비, 글락소스미스클라인, 녹십자, 에스케이플라즈마, 한국로슈, 머크, 바이엘코리아, 한국에자이, 비씨월드제약(200780), 한국피엠지제약, 명인제약, 에리슨제약, 한림제약 등 15개 제약·바이오기업 또한 코로나19 대체 치료 의약품을 공급하고 있다. 리바비린·칼레트라(복합제)·자나미비르·이뮤노글로불린·인터페론·히드록시클로로퀸황산염 등 6개 제품이다.
|
이날부터 식약처는 ‘고강도 신속 제품화 촉진 프로그램’(고(GO)·신속 프로그램) 본격 운영에 들어갔다. 통상 30일가량 소요되는 임상시험 심사 기간을 대폭 줄인다. 사용 경험이 있는 물질은 7일 이내, 신물질의 경우 15일 이내로 심사 기간을 단축한다. 기존에 사용 중인 의약품의 코로나19 치료 효과를 확인하기 위한 ‘약물 재창출’ 임상시험은 7일 이내에 심사를 완료할 계획이다.
업계 관계자는 “코로나19 치료제 및 백신 개발 등에 있어 제약 자국화에 중요한 R&D 지원, 세제 혜택, 신속 심사 등 정부 정책 수단을 총동원해 주시기 바란다”고 건의했다.

.png)