연세대 의과대학 의생명과학부 김현석 교수와 KIST 이철주 책임연구원, 삼성서울병원 남도현 교수 연구팀은 다기관 공동연구를 통해 악성 뇌종양의 예후를 예측할 수 있는 바이오마커와 치료제를 발견했다고 밝혔다.
과학기술정보통신부 포스트게놈다부처유전체사업, 중견연구자지원사업 및 바이오의료기술개발사업과 보건복지부 선도형 특성화연구사업의 지원을 받은 이번 연구결과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications) 최신호에 게재됐다.
교모세포종은 뇌에 발생하는 악성뇌종양 중 가장 흔한 뇌종양이다. 수술적 치료가 가장 중요하며 표준치료로 수술 후 항암치료, 방사선치료 등을 병행하지만 예후가 좋지 않다. 특히 이소시트르산탈수소효소(IDH)에 유전자 변이가 없는 야생형 교모세포종의 경우 전체 교모세포종 중 90%를 차지하는데 예후가 나쁘며 치료제도 없는 것으로 알려져 있다.
교모세포종 예후예측과 맞춤형 치료제 개발을 위해 주로 유전체(DNA), 전사체(RNA) 수준의 연구들이 진행돼왔지만 교모세포종의 예후예측과 치료에는 큰 도움이 되지 못하는 실정이다.
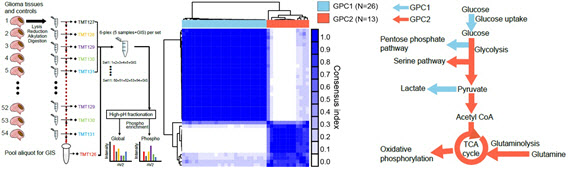
연구팀은 교모세포종 50종의 시료를 질량분석(Mass Spectrometry) 기반 프로테오믹스 방법으로 분석해 최초로 대규모 교모세포종 단백체 데이터를 확보했다. 확보된 단백체 데이터와 동일 시료로부터 수집한 유전전사체에 대해 약물 반응 데이터 통합 분석을 시행했다. 분석결과, IDH 야생형 악성 교모세포종이 당대사, 면역조절, 종양기원이 다른 두 개의 GPC(GBM Proteomic Cluster, 교모세포종 단백체 클러스터) 그룹으로 분류됨을 확인했다.
GPC1의 경우 악성 예후 바이오마커인 FKBP9의 발현이 높고, 종양기원세포의 특성이 강하며 면역관문억제제의 표적인 PD-L1의 발현이 높은 특성이 있다. 반면 GPC2의 경우 좋은 예후 바이오마커인 PHGDH(세린 대합성 대사 효소)의 발현이 높고 대사적으로 산화적인산화 단백질 발현이 높은 특성을 보였다.
|
또한 연구팀은 독립적인 세브란스 교모세포종 코호트연구와 종양구 침윤 실험을 통해 PHGDH 효소 발현에 따른 환자의 예후 및 침윤 정도를 평가했다. 그 결과, PHGDH 발현이 높고, 암줄기 세포 마커인 Nestin 단백질의 발현이 낮은 환자군이 상대적으로 양호한 예후를 보였다. 또한, 교모세포종 암세포에서 PHGDH를 과발현시켰을 때 종양구의 침윤이 유의하게 감소함을 확인했다.

.png)









![30만원짜리 러닝화 왜 신죠?…'반값' 카본화 신고 뛰어봤습니다[신어보니]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/05/PS26050702444t.jpg)

