|
13일 식품의약품안전처에 따르면, 현재 코로나19 진단키트 긴급사용 승인을 받기 위해 정부 검토 과정에 있는 것은 9개 업체의 10개 품목이다.
식약처 관계자는 “모두 임상 과정에 있는 상황이고 업체명은 공개할 수 없다”며 “임상 성능 평가에 따라 긴급사용 승인이 결정될 것”이라고 말했다.
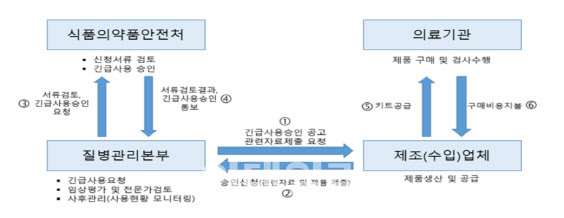
식약처는 질병관리본부와 협력해 서류검토(식약처)→임상 성능평가(질본)→전문가 검토(대한진단검사의학회)→승인요청(질본) 및 승인(식약처) 4단계 검토 절차를 거쳐 긴급사용 승인을 내주고 있다.
앞서 지난 1월 28일부터 2월 28일까지 국내 진단키트 기업 42개 업체에서 질본을 통해 64건에 대해 긴급사용 승인을 신청했다.
이 중 지금까지 코젠바이오텍과 씨젠(096530), 솔젠트, 에스디바이오센서, 바이오세움, 바이오오코아 등 모두 6곳이 긴급사용 승인을 받았다.
분자진단 전문업체 바이오코아의 코로나19 진단 키트가 11일 6번째로 가장 최근에 긴급사용 승인을 획득했다.
이들 제품은 모두 실시간 유전자 증폭 기법 방식(RT-PCR)으로 코로나19를 진단하는 제품이다. 정부는 RT-PCR에 대해서만 긴급사용 승인 문을 열어줬다.
긴급사용 승인 제도는 감염병 대유행이 우려돼 의료기기의 긴급한 사용이 필요하나 국내에 허가제품이 없는 경우 등에 제품 허가를 면제해 한시적으로 제조(수입)·판매·사용할 수 있게 하는 제도다.
질본은 최근 코로나19 응급용 유전자 검사시약 긴급사용을 위한 공고를 추가로 낸 상황이다. 응급환자를 대상으로 1시간 이내에 진단검사 결과 도출이 가능한 제품이 대상이다.
이는 현재 코로나19 확진자 검사에 사용하고 있는 RT-PCR 검사에 6시간 정도가 소요되고 있는 점을 감안한 조치다. 빠른 시간 내 수술이나 처치 등이 필요한 응급환자의 경우 보다 빠른 검사법 활용의 필요성이 제기되고 있기 때문이다.
앞서 정은경 중앙방역대책본부 본부장은 지난달 26일 정례 브리핑에서 “응급환자 발생 시에 신속하게 코로나19 감염을 확인할 수 있는, 1시간 이내에 검사를 할 수 있는 PCR 검사법 도입을 검토하고 있다”고 밝혔다
두번째 긴급사용 승인 신청은 내달 1월부터 5일까지 할 수 있다.
|






![외국행 꿈에 엄마가 걸림돌…친모 살해 뒤 옆에서 잠든 아들[그해 오늘]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/02/PS26021200006t.jpg)

