|
셀리버리(268600)는 매출액 기준 아시아 2위 글로벌 제약사의 요청으로 현재 공동개발중인 유전자간섭 안티센스 올리고핵산 (anti-sense oligonucleotide: ASO) 항암신약의 세포내 전송 및 대장암·폐암·유방암 유발 특정 유전자의 발현억제효능 검증 최종결과보고서를 이 제약사에 공유했다고 13일 밝혔다.
자료를 요청한 해당 제약사는 셀리버리의 플랫폼기술 ‘약리물질 생체 내 전송 TSDT 플랫폼기술’을 활용해 생체전송이 어려운 핵산기반 항암신약을 생체조직 내 세포 안으로 전송시키는 치료신약의 공동개발을 제안했다.
이는 한번 세포에 들어간 올리고핵산 ASO는 다시 세포 밖으로 나오지 못하는 한계 때문에 장기 깊숙한 세포까지 전송시킬 수 없는 문제점을 셀리버리 TSDT 플랫폼기술로 극복해 차세대 핵산기반 항암신약으로 개발하기 위한 목적이다.
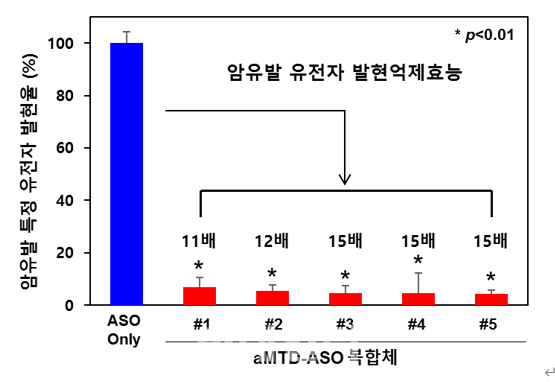
이 글로벌 제약사는 공동개발 마일스톤 1단계 마무리를 위해 지난 2월에 셀리버리가 송부한 중간결과보고서를 면밀히 검토했다. 그 결과 TSDT 플랫폼기술이 적용된 펩타이드-핵산 복합체 (aMTD-ASO conjugate)는 암을 유발하는 특정유전자의 발현을 기존 올리고핵산 ASO에 비교해서 상당수준 억제함을 확인했다고 밝혔다.
이 회사는 계약을 면밀히 검토하기 위해 TSDT 플랫폼 기술이 올리고핵산의 유전자간섭 능력을 향상 시키는지에 대한 작용기전 (mode of action: MoA) 및 기존 올리고핵산 ASO 대비 특정유전자의 발현을 정량적으로 얼마나 더 억제 (Add-On effect) 하는지에 대한 추가 자료를 요청했다. 이에 셀리버리가 응한 것이다.
신슬미 박사는, “이번 2차 (최종)결과보고서에는 이 아시아 2위 제약사가 요청한 25종의 펩타이드-핵산 접합약리물질 (aMTD-ASO conjugates)에 대해 대장암·폐암·유방암을 일으키게 하는 특정 유전자를 얼마만큼 발현을 저해 (넉다운, knockdown: KD activity) 하는지를 정량적으로 검증한 결과가 모두 다 포함됐다”고 설명했다.
신 박사는 “셀리버리의 제3세대 세포막 투과 펩타이드 aMTD가 ASO 올리고핵산에 화학적으로 접합된 aMTD-ASO 접합체는 빠른 시간내에 세포막 직접투과 메카니즘으로 세포내 전송이 가능하디”며 “이 때문에 aMTD가 접합되지 않은 단순 ASO가 전송되지 못하는 조건에서 유전자 발현저해 넉다운 (KD) 활성을 증명했다는 것이 핵심”이라고 강조했다.
그는 인간 폐암세포에서 25종의 aMTD-ASO 접합체의 대장암·폐암·유방암 유발 유전자의 발현저해능력이 단순 ASO 대비 3배 이상의 aMTD-ASO 접합체는 4종, 5배 이상은 10종, 10배 이상은 11종 이며, 최고 15 배까지 특정 유전자 넉다운효능을 갖는 것으로 결과가 도출됐다고 부연했다. 이어 aMTD와 접합된 25종 aMTD-ASO 모두 단순 ASO 보다 최소 3 배 이상 최대 15배까지 암세포 전송시험에서 약리효능을 가짐을 증명했다고 말했다.

.png)