이희영 대신증권 연구원은 “한미약품은 지난 27일 비만 치료제 에페글레나타이드(GLP-1)의 국내 임상 3상 결과를 발표했다. 주요 지표 모두 통계적 유의성을 확보함에 따라 약물 성공 확률 100%를 적용하고 신약가치를 상향 반영했다”며 이같이 밝혔다.
이 연구원은 “향후 자체 생산 기반 가격 경쟁력, 낮은 부작용에 기반한 치료 지속성, 100% 아시아인 데이터로 확보된 높은 시장 적합성 등을 고려할 때 상업적 성공 가능성이 높다고 판단한다”고 말했다.
이어 “한미약품은 올해 12월 국내 허가 신청, 2026년 하반기 국내 출시를 목표로 하고 있다”며 “사노피와 진행했던 당뇨 임상 데이터를 활용해 글로벌 확장 전략도 준비 중”이라고 설명했다.
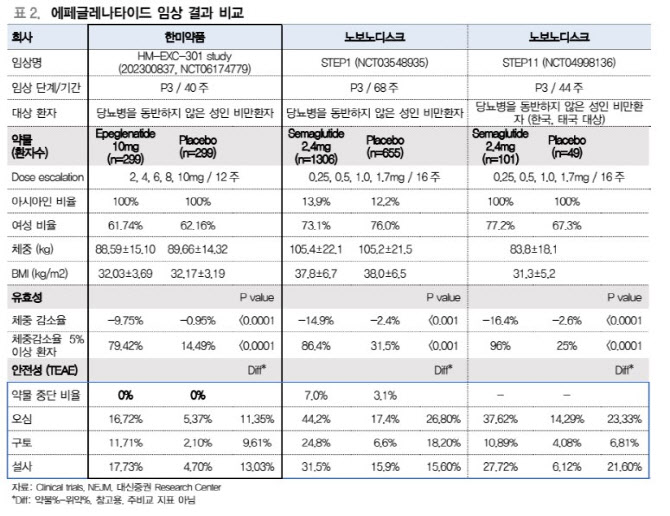
이 연구원은 “한미약품 에페글레나타이드는 국내 임상 3상에서 40주 시점 체중감소율 -9.75%(p<0.0001) 및 ≥5% 감량 환자 비율 79%(p<0.0001)을 확인하며 비만적응증 허가요건을 충족했다”며 “효능은 세마글루타이드 STEP1(-14.9%, 68주, 글로벌) 및 STEP11(-16.4%, 44주, 아시아) 대비 다소 낮으나, 체중 정체기 없이 지속적인 감량 곡선을 보여 64주 연장 데이터에서 추가 감량 기대감이 존재한다”고 분석했다.
그러면서 “안전성 측면에서는 임상 중단율 0% 및 낮은 위장관 부작용이 확인됐다”며 “12주 이내 빠른 용량 도달은 초기 환자 이탈 감소와 장기 처방 유지에 유리하다”고 평가했다.
이 연구원은 “비만 시장이 효능 중심에서 지속 가능성 중심으로 재편되는 흐름을 고려할 때, 에페글레나타이드는 위장관 부작용으로 기존 치료제를 지속하기 어려운 환자군에서 확실한 수요를 확보할 수 있다”며 “여기에 자체 생산 기반의 원가 경쟁력과 100% 아시아인 임상 데이터에 기반한 높은 시장 적합성은 실제 처방 전환과 상업화 속도를 높이는데 일조할 전망”이라고 덧붙였다.
|

.png)