|
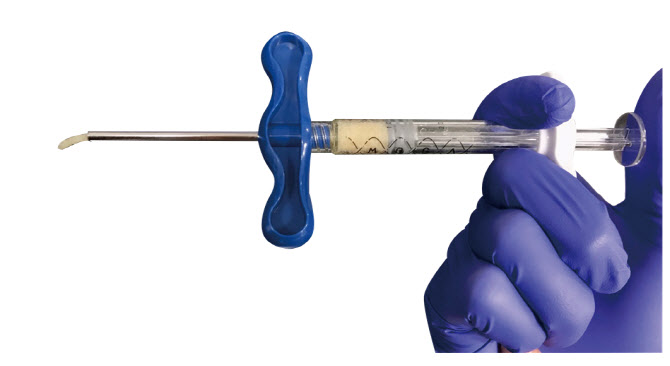
메가카티는 사람의 무릎연골과 동일성분인 초자연골(Hyaline Cartilage)에 성형성과 접합성을 높인 인체연골 유래 융합 의료기기로 손상된 무릎연골에 직접 주입하면 연골재생이 촉진되는 방식이다.
기존 줄기세포를 이용한 연골재생은 주입된 줄기세포가 연골세포로 분화하고, 분화된 연골세포에서 연골성분을 분비해서 연골조직이 만들어지는 긴 과정을 거친다. 반면, 메가카티는 부분절개 또는 관절경 시술로 손상된 연골부위에 실제 인체 연골을 주입하기 때문에 연골 재생 효과가 더 우월하다.
최근에는 시술자의 편의성을 더하기 위해 메가카티 주입기구를 개발해 특허를 출원했고, 메가카티의 시술효과가 더욱 높아질 것으로 기대된다.
메가카티는 2019년 12월에 식품의약품안전처(식약처)부터 임상시험계획 (IND)을 승인받았다. 이듬해 4월부터 2021년 1월까지 연세대 강남 세브란스병원(CI 기관), 연세대 신촌 세브란스병원, 고려대 안암병원, 국민건강보험공단 일산병원에서 총 90명의 임상 피험자를 모집해 시술 후 1년간 추적 관찰을 진행했다.
임상시험 결과 1차 유효성 평가지수인 무릎연골 구조적 재생 평가 방법(MOCART) 점수가 메가카티군에서 대조군인 미세천공술 단독 대비 우월함이 입증됐다. 아울러 2차 평가지수(Kellgren-Lawrence Grade) 에서도 통계적 유의성이 확인됐다.
엘앤씨바이오는 6월 내로 식품의약품안전처에 의료기기 품목허가 (NDA)를 신청해 연내 허가를 획득하고, 내년 상반기 국내 시장에 메가카티를 출시할 계획이다. 이후 국내 제품허가 임상결과와 허가자료를 활용해 중국 국가약품 감독관리국(NMPA)에 허가 신청을 할 계획이다.
이환철 엘앤씨바이오 대표는 “이번 임상시험 결과로 메가카티의 효능과 안전성이 입증된 만큼 식약처로부터 의료기기 허가를 빠른 시일 내에 획득하여 내년 상반기 시판이 가능하도록 만반의 준비를 마쳤다”면서 “메가카티를 필두로 기존 제품인 메가필하이젝트, 메가DBM, 저선량 CT 파이온2.0 등 관절ㆍ척추용 제품들의 중국 진출이 이뤄질 예정”이리고 말했다. 이어 “또 해당 분야 최고 국내 기업들과 전략적 협업을 통해 엘앤씨바이오가 중국 진출 플랫폼을 제공할 것”이라고 덧붙였다.

.png)