|
엄민용 연구원은 “키트루다는 올해 처음으로 3분기 매출만 10조원을 달성했다”며 “머크는 이번 3상 결과로 승인받은 모든 적응증을 승인 가능(로슈 티쎈트릭SC도 3상 한 번으로 모든 적응증 승인)하다. 50% 이상의 SC전환 추정 확실시됐다”고 판단했다.
엄 연구원은 “기존 키트루다 IV(혈관주사)는 짧게는 30분에서 2시간 투약이나 SC는 평균 2~3분 내 투약 가능해 의료진과 환자의 편의성 개선뿐 아니라 입원비용 감소로 각국의 의료보험 재정지출 감소 효과까지 기대된다”며 “자세한 데이터는 곧 학회로 발표될 예정이며 1월 중으로 전세계 허가 신청이 추정된다”고 봤다.
그는 “피하주사 원료 생산 위한 공장증설도 머크 요청으로 추정된다”며 “국내 바이오텍 중 상업화에 성공한 최초의 기술플랫폼 보유 기업이자 공장까지 갖추는 첫 회사 될 것이다. 기술이전 논의 중인 6개의 빅파마도 의사결정 쉬워질 것”이라고 진단했다.
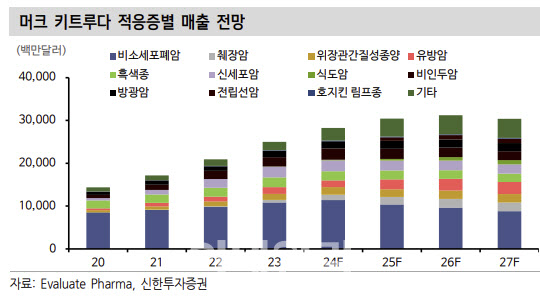
엄 연구원은 “머크가 키트루다SC를 2028년까지 50% 시장을 전환을 목표로 발표했고 2030년까지 전환율은 지속 증가해 연간 20조~30조원 수준 매출이 추정된다”며 “3상 성공 발표로 단계별 마일스톤 1조 4000억원은 출시 후 2년 내 모두 인식 가능할 것이다. 판매 로열티 4~5% 가정 시 연간 1조원 이상 인식도 기대된다”고 강조했다.


.png)
.png)








![[그해 오늘]38명 목숨 앗아간 이천 화재…결국 '인재'였다](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042900001t.jpg)

