젬백스앤카엘로부터 진행성핵상마비(PSP) 치료제 ‘GV1001’를 도입한 삼성제약도 주가가 상한가를 기록했다. 대화제약도 이날 중국 시장 진입 가속화 가능성이 제기되면서 상한가에 근접한 급등세를 나타냈다.
|
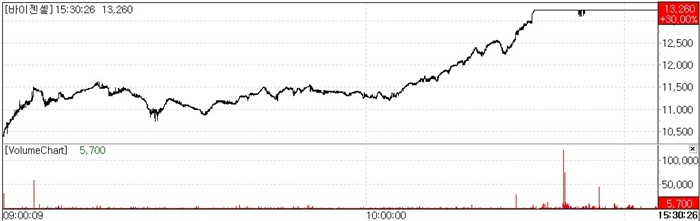
바이젠셀, 1111 거래일 연속 주가 상승세
8일 KG제로인 엠피닥터(MP DORTOR·옛 마켓포인트)에 따르면 바이젠셀(308080)은 이날 주가가 전일 대비 30%(3060원) 오른 1만3260원을 기록했다. 최근 바이젠셀은 11거래일 연속 주가 상승세를 나타냈다. 11월 24일 전일 대비 140원 오른 3270원을 기록한 후 이날까지 주가가 상승했는데, 신약 임상 2상 성공 소식 후 향후 모멘텀에 대한 기대 심리가 상한가까지 이끌었다는 분석이다.
실제로 바이젠셀은 지난달 25일 NK/T 세포림프종 치료제로 개발 중인 ‘VT-EBN-N’ 임상 2상 톱라인 데이터를 발표했다. 투약 완료 후 2년간의 경과 관찰에 대한 수치가 핵심인데 임상적 유효성과 안전성을 입증했다.
서울성모병원을 포함한 전국 13개 의료기관에서 환자 48명을 대상으로 무작위배정·이중맹검 방식으로 진행된 임상 2상에서 1차 유효성 평가 변수인 2년 무질병생존(DFS)에서 투여군은 95.0%, 대조군은 77.58%로 나타났다. 두 군 간 차이는 통계적으로 유의미(p=0.0347)한 것으로 분석됐다.
투여군에서는 재발 또는 사망 등 이벤트 발생률이 4.76%(1명)에 불과했다. 대조군은 32%(8명)로 나타났다. 이번 결과는 VT-EBV-N이 NK/T세포 림프종 환자의 장기 질병 억제에 의미 있는 효과를 보여준 것으로 평가받는다.
특히 바이젠셀은 임상 2상 성공으로 조건부 허가 절차를 밟을 것으로 전망된다. 이미 회사는 해당 치료제에 대해 식품의약품안전처로부터 2019년 희귀의약품 지정을 받았다. 희귀의약품 지정을 받으면 품목허가 심사에서 우선 심사를 받을 수 있어, 허가까지 기간을 단축할 수 있다.
이와 함께 대체 치료제가 없거나 생명이 위중한 질환으로 인정받을 경우 조건부 허가 신청도 가능하다. 투심은 신속한 상업화와 이에 따른 실적 모멘텀에 주목하고 있다. 바이젠셀 측은 상용화 5년 내 1000억원대 이상의 매출을 기대하고 있다. 아울러 바이젠셀은 중국 기업과 기술이전 협상도 재개할 것으로 예상된다.
바이젠셀 측은 내년 상반기 정도에 신속처리 지정을 신청하고 이후 조건부 허가 신청을 계획하고 있다. 바이젠셀 관계자는 “금일 상한가는 지난달 세포림프종 치료제 임상 2상 결과 발표가 영향을 준 것으로 보고 있다. 임상 2상 후 모멘텀에 대한 투심이 작용한 것으로 판단한다”며 “그동안 회사 주가가 저평가돼 있던 부분도 영향을 끼친 것으로 보고 있다”고 말했다.
그러면서 “VT-EBV-N 임상 2상 최종 결과보고서(CSR)는 내년 초에 나올 예정으로 CSR을 수령 후 상반기에 식약처에 신속처리 지정 신청을 하고 하반기에 조건부 허가를 신청할 것”이라며 “조건부 허가를 획득하면 세계 최초 NK/T 세포치료제를 상용화하게 된다"고 말했다.
이어 "2027년 상용화를 예상하고 상용화 5년 차인 2031년에는 1200억원대 매출을 기대하고 있다"며 "과거부터 진행하던 중국 기업과 기술이전 협의도 재개할 예정”이라고 설명했다.
PSP 치료제 ‘GV1001’ 도입한 삼성제약, 적응증 확장 기대감
최근 젬백스(082270)앤카엘은 삼성제약(001360)에 진행성 핵상마비(PSP) 치료제 ‘GV1001’을 기술이전 했다. 아시아 주요 4개국에 대한 임상 개발 및 상업화 권리를 선급금 115억원 포함 총 2200억원에 넘겼다.
이번 계약으로 삼성제약은 기존 알츠하이머를 적응증으로 한 GV1001에 이어 PSP 치료제까지 확보했다. 특히 한국, 일본, 인도, 인도네시아에 대한 권리를 획득하면서 파이프라인 강화와 글로벌 진출 국가 수를 늘렸다는 평가다. 이날 삼성제약 주가도 껑충 뛰었다. 직전 거래일 1364원이던 주가는 8일 상한가인 29.99%(409원) 오른 1773원으로 장을 마감했다.
젬백스에 따르면 PSP 치료제 GV1001은 국내 2상 임상시험에서 우수한 내약성과 함께 질환 진행 속도를 늦추는 경향성을 보여준 바 있다. 이어서 진행된 12개월 연장 임상시험까지 합산한 72주 데이터 분석에서는 진행성핵상마비 리처드슨 신드롬(PSP-RS) 유형 환자군을 대상으로 PSP 등급 척도(PSP-rating scale)의 총점 변화량을 분석한 결과, 저용량(0.56mg)군에서 외부 대조군 대비 통계적 유의성을 확인했다.
삼성제약 관계자는 “젬백스로부터 PSP 치료제를 도입하면서 알츠하이머 치료제에 이어 적응증 확장을 했다는 의미가 있다”며 “파이프라인 확장에 대한 모멘텀과 상용화에 대한 기대감이 작용하면서 주가가 강세를 보인 것으로 보고 있다”고 말했다.
제약업계에서는 현재 젬백스가 추진 중인 PSP 치료제 임상 3상이 본격화하고 삼성제약이 판권을 확보한 한국과 일본, 인도, 인도네시아가 글로벌 임상 3상 사이트에 포함된다면 임상 3상 개발에 중추적인 역할을 할 수 있을 것으로 보고 있다.
대화제약, 마시는 항암제 中서 가격 경쟁력 확보
대화제약(067080)은 이날 경구용(마시는) 파클리탁셀 항암제 ‘리포락셀’이 중국 국가의료보장국(NHSA)이 발표한 2025년 국가급여의약품목록(NRDL)에 신규 등재됐다고 발표했다. 발표 직후 주가가 급등해 직전 거래일 대비 21.02%(4030원) 오른 2만3200원을 기록했다.
대화제약 관계자는 “리포락셀이 중국에서 국가급여의약품목록에 등재되면서 주가가 영향받은 것으로 보고 있다”고 말했다. 리포락셀은 정맥주사 제형의 항암제를 경구용으로 제형을 변경한 개량 신약으로 지난해 9월 중국 국가약품감독관리국으로부터 위암 적응증으로 품목허가를 획득했다.
올해 1월부터 비급여 판매가 이뤄졌지만 이번 보험 등재로 가격 경쟁력을 확보했다. 보험 적용으로 리포락셀은 300mg 기준 1208위안(약 25만원)의 약가가 확정됐다. 가격 경쟁력을 확보한 만큼 중국 시장에서 시장점유율 확대에 속도가 붙을 것이란 평가가 제기된다.
대화제약 관계자는 “리포락셀액의 NRDL 등재는 대화제약의 기술력과 치료 혁신성을 중국 의료 시장에서 공식적으로 인정받은 중요한 성과”라며 “파트너사와의 긴밀한 협력을 통해 현지 시장에서의 실행력을 강화하고 글로벌 항암제 시장에서 대화제약의 위상을 한 단계 더 높이겠다”고 말했다.


.png)
.png)






![[르포]베이징 들썩였다…현대차 아이오닉V 공개현장 ‘인산인해'](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042401039t.jpg)


