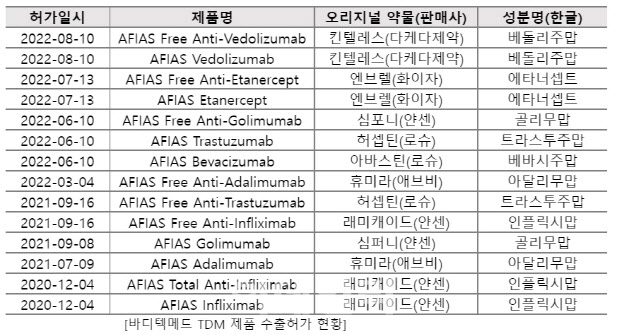
바디텍메드는 16일 식품의약품안전처로부터 TDM 진단키트 △AFIAS Vedolizumab △AFIAS Free Anti-Vedolizumab △AFIAS Etanercept △AFIAS Free Anti-Etanercept에 대한 수출허가를 획득했다고 밝혔다. 이번 승인으로 수출허가를 획득한 TDM 진단키트는 총 14종으로 확대됐다.
TDM은 약물 투여 후 해당 약물이 치료적인 범위 내에 있는지 또는 약물 투여 후 몸 속 면역반응 발생 여부를 확인하는 검사다.
AFIAS Vedolizumab(베돌리주맙)은 중증의 활성 궤양성 대장염이나 크론병 치료를 받는 환자에게 투여되는 베돌리주맙의 혈중 농도를 측정하는 진단키트다. AFIAS Free Anti-Vedolizumab은 베돌리주맙 투약 후 면역반응에 의한 항체의 생성여부를 측정하는 진단키트다.
|
킨텔레스와 엔브렐은 적응증 확대와 환자수 증가에 따라 수요가 증가될 전망이다. 킨텔레스는 지난해 1월 궤양성대장염에 대한 1차 치료제로 적응증을 확대했다. 엔브렐은 전세계 국가에서 인구 고령화가 가속화되면서 관절염을 비롯한 각종 질환의 진단을 필요로 하는 환자가 늘고 있어 제품 수요 또한 증가할 전망이다.
바디텍메드는 혈중 약물의 농도와 면역반응 확인을 위한 검사에 소요되는 시간을 3주에서 12분으로 줄인 TDM제품을 개발해 공급 중이다. 임상적 성능은 기존 방식과 유사한 수준을 유지하면서 시간은 단축해 환자 편의성을 높였다.
최의열 바디텍메드 대표이사는 “이번 수출허가 추가 승인으로 TDM 사업에 속도가 붙고 있다”며 “환자 편의성과 제품의 정확성 등을 강조한 적극적인 마케팅 활동과 동시에 추가 공급사 확보에 총력을 다해 글로벌 TDM 시장을 선도하는 기업으로 도약하겠다”고 밝혔다.



!['과대망상'이 부른 비극…어린 두 아들 목 졸라 살해한 母[그해 오늘]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/02/PS26021700001t.jpg)
