|
버텍스, 오름의 TPD² 어떻게 활용할까?
17일 이승주 오름테라퓨틱 대표는 이데일리에 “유전자가위 치료제의 안전한 전처리제 개발에 오름이 가진 TPD² 플랫폼이 유효할 것이라고 봤고, 이번 계약을 위한 버텍스와의 미팅에서는 이런 점을 강조했다”며 “버텍스는 오름의 TPD² 기술로 개발한 DAC에 대해서만 독점 권리를 갖고 있어 이번 계약 이후 다른 크리스퍼-카스9 회사와의 TPD²를 통한 협업 가능성은 열려 있다”고 말했다.
오름은 전날 버텍스와 글로벌 다중 타깃 라이선스 및 옵션 계약을 체결했다. 3개 타깃에 대해 각각 최대 3억1000만 달러(약 4000억원)의 마일스톤을 받을 수 있으므로 1500만 달러(약 200억원)의 업프론트(선급금)까지 더하면 총 계약 규모는 9억4500만 달러(약 1조3000억원)에 달한다.
버텍스는 세계 최초 크리스퍼-카스9 유전자가위 치료제 상용화 기업으로 알려진 곳이다. 오름의 앞선 딜에서 급성골수성백혈병(AML) 치료제 ORM-6151를 1억8000만 달러에 사간 BMS보다 시총 규모는 1.5배 가까이 더 크다(17일 기준 시총 △BMS(BMY) 875억 달러 △버텍스(VRTX) 1260억 달러).
버텍스는 지난해 연말 영국과 미국, 유럽에서 잇따라 세계 최초 유전자가위 치료제의 승인에 성공했다. 이 약물의 이름은 ‘엑사셀’(미국명)로, 겸상적혈구증후군 및 베타지중해 빈혈이라는 희귀질환을 타깃으로 한다. 유전자 이상으로 발생하는 이 질환을 엑사셀은 크리스퍼-카스9 유전자가위로 교정해 치료하는 것이다.
치료는 골수 이식과 유사한데 환자로부터 혈액 줄기세포(조혈모세포)를 채취해 문제 부위를 유전자가위로 교정하고 다시 생착시키는 과정을 거친다. 1회 투약 비용이 220만 달러(약 30억원)에 달하지만 아직까지 주기적 수혈 외에는 별다른 치료옵션이 없어 한 번의 치료로 영구적인 효과 유지가 기대되는 엑사셀이 허가될 수 있었다.
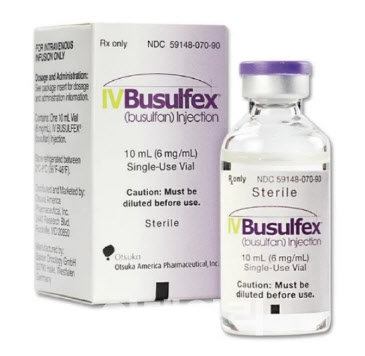
하지만 엑사셀을 통한 치료 과정은 부작용 위험이 높다. 엑사셀 자체로 인한 부작용보다는 엑사셀 투여 전, 투여를 위한 환경을 조성하는 전처리작업에서 특히 높다. 교정된 줄기세포를 환자의 몸에 다시 이식하기 전 며칠 동안 환자에게 ‘부설판’이라는 화학항암제를 투여해 교정된 줄기세포가 자리잡을 수 있도록 환자의 오래된 세포를 죽이는 전처리작업이 진행되는데 이 과정에서 부작용이 나타나는 것이다.
|
부설판의 대표적인 부작용으로는 골수 억제로 인한 감염, 빈혈 및 출혈 위험 증가, 폐 손상, 간 손상, 장 점막 손상, 탈모, 백혈병과 같은 2차 악성 종양 위험 등이 꼽힌다. 실제로 엑사셀 임상시험 과정에서도 한 환자가 폐렴 및 호흡부전으로 사망했는데, 당시 사망 원인 중 하나는 부설판으로 인한 폐 손상이었고 엑사셀과는 관련이 없다고 평가됐다.
특히 버텍스는 부설판의 부작용 중 불임 때문에 골머리를 앓아왔다. 버텍스는 현재 미국에서 엑사셀을 투약하는 상업보험 가입 환자에게는 최대 7만 달러(약 1억원)의 불임치료 비용을 부담하고 있다.
이승주 대표는 “엑사셀 투여 환자가 전처리과정을 겪으면서 불임이 되는 경우가 많은데, 부설판이 아닌 표적 전처리제를 사용한다면 이 문제를 해결할 가능성이 있다”며 “TPD²를 활용해 기존 화학항암제를 보다 표적화된 것으로 대체하려는 것”이라고 설명했다.
ADC에 TPD 더했다는 오름의 ‘TPD²’는 무엇?
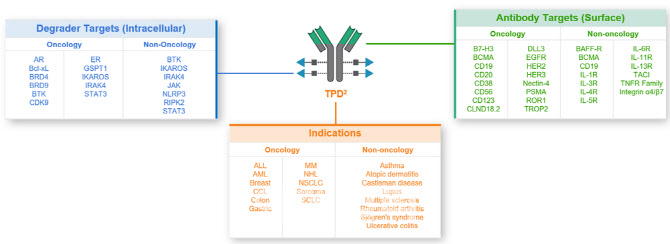
버텍스가 이번에 계약한 오름의 TPD² 기술은 최근 항암제 개발에서 가장 주목받는 항체-약물접합체(ADC) 기술에 차세대 기술인 표적단백질분해제(TPD) 기술을 결합한 것이다. TPD로 약효는 높이고 ADC로 독성은 낮추는 것이 결합의 목적이다.
ADC는 유도미사일 역할을 하는 ‘항체’에 ‘링커’를 통해 폭탄 역할을 하는 ‘화학항암제’(페이로드)을 붙이는 반면, DAC는 문제단백질의 활동을 저해하는 일반적인 세포독성약물 대신, 특정 표적만을 겨냥해 아예 제거해버리는 TPD를 결합해 약효를 높인다.
DAC는 ADC와의 결합으로 TPD의 독성 문제도 개선할 수 있다. TPD는 표적단백질을 골라내 분해하는 장점이 있지만 정상세포 속 표적단백질도 분해할 수 있어 표적(on-target) 독성 위험이 있다. 하지만 ADC의 항체가 TPD를 암세포에 정밀하게 전달하면 안전성을 높이는 효과가 나타난다.
오름은 TPD² 플랫폼 외 PROTAb이라는 링커 플랫폼도 보유하고 있어 향후 추가적인 기술수출 가능성도 기대된다. 오름측 설명에 따르면 TPD²에 PROTAb 링커를 활용하면 TPD의 표적 전달이 강화돼 다양한 단백질분해제를 광범위한 적응증에 DAC로 적용할 수도 있다. 오름은 TPD² 기술을 활용해 치료제를 개발할 수 있는 암 외 적응증으로는 천식, 루푸스, 다발성경화증, 쇼그렌 증후군, 궤양성대장염, 아토피피부염 등을 제시하고 있다. 주로 경구약으로 개발되는 기존의 TPD가 세포투과성과 경구생체이용률이 낮아 다양한 단백질분해제를 활용하지 못한다는 점을 개선한 것이다.
|
이 대표는 “TPD²와 PROTAb을 활용하면 암이 아닌 다른 적응증을 겨냥한 약물도 개발할 수 있는데, 오름은 항암제 개발에 집중하고 그 외 적응증의 치료제에 대해서는 좋은 파트너사와 협력해 개발하는 방향을 취할 것”이라고 했다.
한편, 이번 기술이전 계약 성사로 오름의 코스닥 상장 가도에도 청신호가 켜졌다. 앞서 기술성평가에서 A, BBB 등급을 획득한 오름은 지난달 한국거래소에 코스닥 상장을 위한 상장예비심사를 청구했다.


.png)
.png)









![서울시장 후보 사는 집은…오세훈 ‘대치'vs정원오 ‘왕십리'[누구집]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042600079t.jpg)
![세금 100만원 걷는데 5500원 썼다…국세청 직원 1명이 175억 징수[세금GO]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042600280t.jpg)