17일 삼성바이오에피스는 자가면역질환 치료제 ‘베네팔리’가 유럽연합집행위원회(EC, European Commission)으로부터 최종적으로 시판 허가를 받았다고 밝혔다. 지난 2014년 허가를 신청한지 1년 1개월만에 최종 승인을 받았다.
베네팔리는 지난해 9월 국내허가를 받은 삼성바이오에피스의 첫 바이오시밀러 ‘브렌시스’와 같은 제품이다. 류마티스관절염 등에 사용되는 ‘엔브렐’과 동일한 ‘에타너셉트’ 성분의 제품으로 엔브렐 바이오시밀러 제품 중 세계 최초로 유럽 허가를 받았다.
엔브렐은 세계 시장에서 연간 약 10조원어치 팔리고 있다. 유럽에서는 약 3조원 규모의 시장을 형성 중이다.
이번 최종 허가를 통해 베네팔리는 순차적으로 EU 회원국 28개 국가와 노르웨이, 아이슬란드, 리히텐슈타인 등 유럽 경제공동체(EEA, European Economic Area) 3개국에서 판매가 이뤄질 예정이다.
이로써 삼성은 지난 2010년 5월 바이오의약품을 신수종 사업으로 발표한 이후 약 6년만에 자체개발한 바이오의약품을 세계 시장에 내놓는데 성공했다. 삼성바이오에피스는 지난달 류마티스관절염 등에 사용되는 ‘레미케이드’의 바이오시밀러 ‘렌플렉시스’의 국내 허가를 받았고 지난해 3월 유럽 허가를 신청한 바 있다. 또 추가로 4개의 바이오시밀러를 개발 중이다.
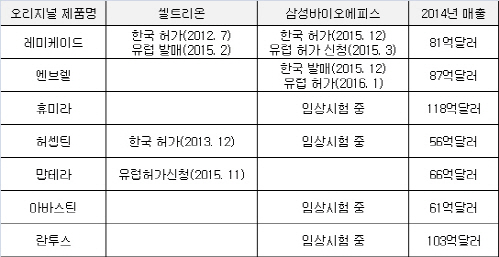
특히 베네팔리의 유럽 허가로 셀트리온과 삼성바이오에피스 등 국내업체 2곳이 글로벌 자가면역치료제 ‘레미케이드’와 ‘엔브렐’의 바이오시밀러를 세계에서 가장 먼저 내놓은 성과를 거두게 됐다.
램시마는 레미케이드의 첫 바이오시밀러 제품으로 지난 2013년 8월 유럽 허가를 받았고, 올해 상반기 미국 시판 승인이 유력하다.
고한승 삼성바이오에피스 사장은 “올해는 삼성바이오에피스가 글로벌 바이오제약 회사로 한 단계 도약하는 중요한 해가 될 것이다”면서 “가격 경쟁력이 있는 베네팔리의 출시를 통해 유럽의 많은 국가들의 의료 재정 향상에 기여하고, 더 많은 자가면역질환 환자들이 치료 받을 수 있을 것으로 기대한다”고 말했다.
|
▶ 관련기사 ◀
☞삼성바이오에피스, 유럽서 첫 바이오시밀러 시판 승인
☞[마감]'전강후약' 코스닥, 이틀째 하락…680선 내줘
☞[마감]코스닥, 쏟아지는 악재에 하락반전…680선은 지지


.png)
.png)





![그 셔츠 제발 넣어입어요…주우재·침착맨의 출근룩 훈수템[누구템]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042500186t.jpg)


![지인에 맡긴 아이 사라졌다…7년 만에 밝혀진 진실[그해 오늘]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042500002t.jpg)
