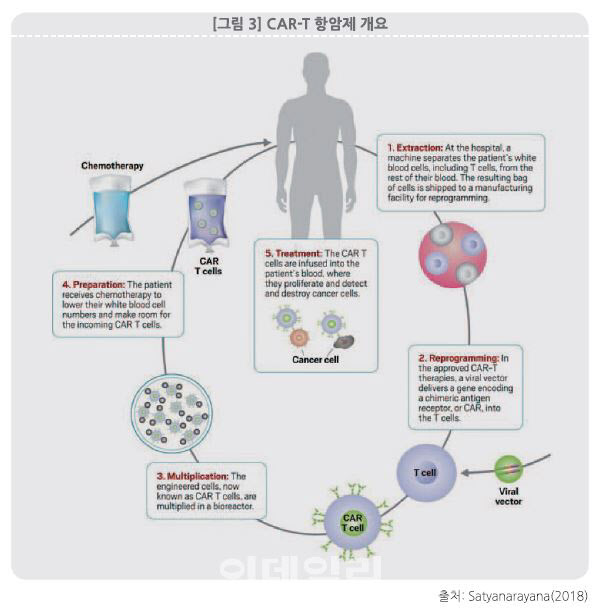
한국바이오협회 ‘면역세포치료제 상용화 동향’ 리포트에 따르면 국내 면역세포치료제 시장도 성장이 예상된다. 지난해 9월 ‘첨단재생의료 및 첨단바이오의약품 안전 및 지원에 관한 법률(이하 첨단재생바이오법)’이 시행된 이후 올해 5월 노바티스 킴리아가 제1호 첨단바이오의약품으로 식품의약품안전처 허가를 획득했다. 4월에는 큐로셀이 미만성거대B세포림프종 치료 후보물질로 국내 기업 최초로 CAR-T 치료제 임상시험을 개시했다.
첨단재생바이오법에 따르면 세포치료제는 첨단바이오의약품 중 하나로 사람 또는 동물의 살아있는 세포를 체외에서 배양 증식하거나 선별하는 등 물리적, 화학적 또는 생물학적 방법으로 조작해 제조한 의약품이다.
|
면역세포치료제 개발은 크게 다섯 가지 방향으로 전개되고 있다. 첫 번째가 효능 강화인데, CAR-T 치료제의 항암 효능 강화를 위해 키메라 항원 수용체 개발이 이뤄지고 있다. 두 번째는 안전성 강화다. 킴리아와 예스카타를 포함 B세포 표면에 발현되는 CD19를 표적하는 CAR-T 치료제들이 보이는 3가지 부작용(B세포 무성형증, 사이토카인방출증후군, 신경독성) 감소나 방지를 위한 개발이 이뤄지고 있다.
세 번째는 적응증 확대다. CAR-T 치료제 개발은 가장 먼저 효능이 입증된 혈액암 중심으로 활발하다. 그간 혈액 종양세포 특이적으로 과다 발현되는 CD19 및 CD20을 표적으로 개발됐으나, 점차 표적 범위가 CD30, BCMA 같은 새로운 표적으로 확대되고 있다. 국내에서 CAR-T 치료제 첫 임상을 시작한 큐로셀은 PD-1과 TIGIT 두 종류의 면역관문수용체 발현을 현저히 낮추는 기술을 개발했고, 적응증을 고형암으로 확대하는 것을 목표로 하고 있다.
네 번째는 동종유래 면역세포치료제 개발이다. 그동안 환자 면역체계에서 높은 호환성을 보이는 자가유래, 즉 환자 자신의 세포를 이용한 면역세포치료제가 많이 개발됐다. 하지만 자가유래 치료제는 투약에 필요한 1~2백만 개 세포 규모의 충분한 양의 건강한 세포를 얻는 게 매우 어렵다. 가격이 동종유래 치료제보다 5~10배 정도 비싸고, 생산과 물류 네트워크도 복잡하다. 동종유래 치료제는 건강인의 세포를 통해 기성품 형태의 치료제를 상용화하는 것이다. 다양한 배치 규모 생산이 가능해 생산비용이 절감되고, 1회 투약 비용이 7500달러로 낮아질 수 있다.
다섯 번째는 선천성 면역세포 NK세포(자연살해세포) 활용이다. NK세포에 CAR를 발현시켜 표적 기능과 활성을 강화한 CAR-NK 치료제는 후천성 면역 세포인 T세포 활용의 한계 및 상용화 관련 저해 요소를 회피할 수 있는 대안으로 개발되고 있다.

.png)