3일 한국바이오협회 ‘블록버스터 의약품 미국 내 제네릭 경쟁 시작’ 리포트에 따르면 다수 블록버스터 약물들이 특허 만료로 미국 내 제네직 제품과 경쟁에 직면한 상황이다.
혈액암 치료제 레블리미드(BMS)가 이스라엘 테바의 제네릭 제품과 미국에서 경쟁이 시작됐다. 레블리미드는 BMS가 2019년 셀진을 인수하면서 권리를 획득한 의약품으로, 지난해 128억 달러의 매출을 기록할만큼 세계에서 가장 많이 팔리는 의약품 증 하나다. 셀진은 레블리미드에 대해 106건에 달하는 특허 출원과 유통을 제한하는 REMS(Risk Evaluation and Mitigation Strategy) 프로그램을 활용, 10개의 개별특허를 통해 제네릭 경쟁을 억제해왔다.
테바는 지난 3월 7일 5㎎, 10㎎, 15㎎, 25㎎ 용량의 첫번째 제네릭을 미국서 출시한다고 발표했다. 리블리미드 특허는 2027년 만료되지만 제한된 양으로 판매를 허용하는 합의를 통해 2022년 3월 이후 제네릭 판매가 가능한 상황이기 때문이다.
국내 기업과 경쟁이 예상되는 블록버스터 제품도 있다. 제넨텍이 개발해 로슈가 권리를 인수한 황반변성 치료제 루센티스는 올해 6월부터 제네릭과의 경쟁에 돌입한다. 루센티스는 미국서 13억5000만 달러, 미국 외 지역서 21억6000만 달러의 매출을 기록한 블록버스터 약물이다.
루센티스에 가장 먼저 대항하는 제네릭 제품이 삼성바이오에피스가 개발한 바이오시밀러 바이우비즈(BYOOVIZ)다. 회사는 올해 6월 루센티스 바이오시밀러를 세계 최초로 출시할 예정이다. 로슈는 루센티스가 독점권을 상실함에 따라 연간 6회가 아닌 3회 주사가 가능한 바비스모(Vabysmo) 허가를 받고 대응을 준비하고 있다.
|
제네릭, 美 시장 진입 평균 12.5년 소요
제네릭 제품의 등장은 블록버스터 의약품 개발사들을 긴장시킨다. 리포트에 따르면 제네릭 진입 첫해 평균적으로 오리지널 의약품 시장점유율이 100%에서 약 12%가 감소한 것으로 나타났다. 또한 매출이 2억5000만 달러를 초과하는 품목의 경우 감소율은 약 7%로 보고된다.
오리지널 의약품 개발사들은 제형, 조성물, 용도, 제조방법 특허 등을 통해 특허 진입장벽을 구축한다. 한 보고서에 따르면 미국 상위 12개 약물 중 절반 이상이 100개 이상의 특허를 신청했거나 획득했다. 미국은 신약 승인 후 5년까지 제네릭의약품 허가 신청을 허락하지 않는다.
또한 미국 식품의약국(FDA)는 희귀의약품, 신규 항생제, 소아용의약품 등 특정 목적을 위해 3년~7년 범위의 다른 규제 독점기간을 부여할 수 있다. 따라서 FDA 승인한 혁신신약은 평균 12.5년 동안 제네릭 경쟁을 방어한 것으로 나타났다.
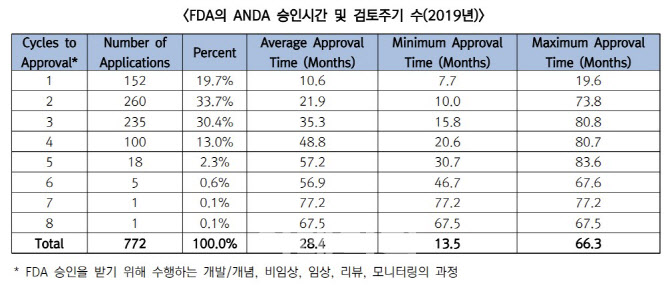
한편 제네릭의약품 심사기간은 평균 28.4개월이 소요되는 것으로 나타났다. 2019년 기준 제네릭 허가신청서(ANDA) 제출추터 승인까지의 평균 시간은 28.4개월이고, 평균 2.47의 사이클이 요구된다. 약 20%는 첫 사이클에서 수신없이 승인을 획득한다.
제네릭의약품은 FDA 허가를 위해 두 종류의 비용도 내야 한다. ANDA 신청에 따른 기본 심사수수료는 2022년 기준 약 2.7억원이며, 원료의약품 등록 및 시설에 따라 정해진 비용(DMF)를 지불해야 한다.


.png)
.png)





![한화 美 필리조선소, 하반기 확장 공사 돌입…마스가 속도전[only 이데일리]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042600922t.jpg)

![서울시장 후보 사는 집은…오세훈 ‘대치'vs정원오 ‘왕십리'[누구집]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042600079t.jpg)
![세금 100만원 걷는데 5500원 썼다…국세청 직원 1명이 175억 징수[세금GO]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26042600280t.jpg)