|
18일 SK바이오팜에 따르면, 엑스코프리(국내명 세노바메이트)는 올 상반기 미국에서 약 720억원의 매출액을 기록했다. 엑스코프리는 지난해 미국에서 매출 782억원(유럽 기술수출료 및 로열티 제외)을 올렸다. 에스코프리의 지난해 미국 매출액은 지난 2020년 대비 6배 증가했다.
그럼에도 엑스코프리는 현재 미국 시장에서 적자를 기록 중이다. 매년 3200억원에 달하는 판매관리비가 발목을 잡고 있기 때문이다. 판관비엔 영업활동비를 비롯해 임상비용, R&D(연구개발)비용, 마케팅 비용 등이 포함된다.
보수적으로 봐도 내년 3분기 흑자전환
엑스코프리는 늦어도 내년 하반기 미국 시장에서 분기 흑자전환이 가능할 전망이다.
SK바이오팜 관계자는 “엑스코프리의 매출 성장 속도를 보면, 보수적으로 봐도 내년 3분기엔 분기 흑자전환이 가능해 보인다”고 말했다.
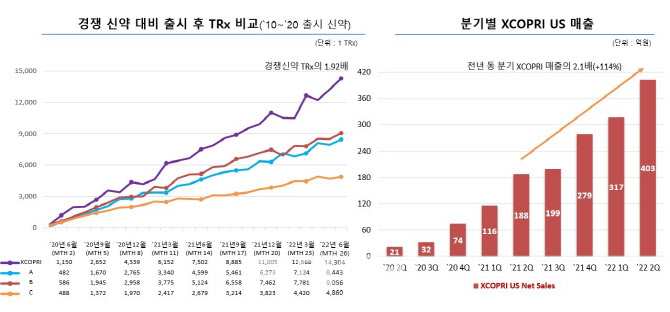
엑스코프리 미국 매출액 동향을 살펴보면 지난해 1분기 116억원 → 2분기 188억원 → 3분기 199억원 → 4분기 279억원 → 올해 1분기 317억원 → 올 2분기 403억원 순으로 증가했다. 현 추세면 엑스코프리가 내년 3분기, 늦어도 4분기엔 손익분기점을 넘어설 수 있단 계산이다.
영업환경 개선에 대한 기대치도 높다. 현재 미국에선 코로나19 재확산으로 약 30%의 병원에 영업사원 출입이 막혀있다. SK바이오팜 관계자는 “영업은 대면·비대면·학술마케팅이 모두 원활하게 돌아가야 처방 건수가 늘어난다”면서 “현재 대면 영업의 어려움으로 기대만큼 매출액이 늘고 있지 않다. 올 하반기부턴 영업환경 개선으로 엑스코프리 처방건수도 동반 증가할 것”이라고 내다봤다.
코로나19 바이러스의 위력 약화와 치료제 공급 확산에 따른 대면 영업 환경이 나아질 것이란 분석이다. 아울러 SK바이오팜은 유명 인사들의 엑스코프리 처방 사례를 SNS와 TV를 통해 광고할 계획이다.
|
◇ 빔팻 특허만료로 처방건수 증가 전망
부동의 1위 치료제인 ‘빔팻’의 특허만료에 따른 수혜도 기대된다. UBC의 빔팻이 지난 3월 17일 자로 특허가 만료됐다. 빔펫은 지난해 매국 시장에서 12억7000만달러(1조5904억원) 매출을 기록했다. 미국 뇌전증 치료제 시장에서 수년간 매출액 1위를 차지했다.
SK바이오팜 관계자는 “빔팻 특허만료로 제네릭(복제약)이 쏟아지고 있다”면서 “약가가 비싼 오리지널 빔팻 대신 약가가 저렴한 빔팻 제네릭과 엑스코프리를 동시 처방받는 경우가 늘고 있다”고 밝혔다. 이어 “자연스레 엑스코프리가 미국 사보험을 적용받는 건수가 증가하고 있다”고 덧붙였다.
오리지널 뇌전증 치료제 평균 약가는 한달 기준 1000달러(130만원) 내외다. 엑스코프리 약가는 여타 오리지널 의약품보단 저렴하다. 그 결과, 환자 제네릭과 엑스코프리를 동시 처방받아도 약가는 기존 오리지널 약가와 대응한 수준으로 알려졌다. 환자들은 기존 치료제를 이용하면서도 상대적으로 치료 효능이 높다고 알려진 신약을 복용할 기회가 생기는 셈이다.
미국 사보험은 신약부문 예산이 한정돼 복수의 신약 복용에 대해선 의약품 구매비를 지원하지 않는다. 이 때문에 환자들은 빔팻 특허만료 전 빔팻과 엑스코프리를 놓고 양자택일할 수밖에 없었다. 하지만 빔팻이 특허만료되면서 엑스코프리와의 관계가 ‘경쟁’에서 ‘상호 보완’으로 재설정됐다는 분석이다.
이날 기준 미국 식품의약국(FDA)로부터 승인받은 빔펫 제네릭 의약품은 14개사 56품목에 이른다.
2025년 환자군과 시장 동시 확대
중장기적으로 엑스코프리는 환자군 확대와 시장 확대로 매출 확대를 꾀하고 있다. 엑스코프리는 현재 만 18세 이상 성인을 대상으로 FDA 품목허가를 받았다. 소아와 청소년에겐 처방이 불가능한 상태다. SK바이오팜은 현재 엑스코프리에 대해 미국 소아 임상 3상을 진행 중이다. 소아 임상에 성공하면 엑스코프리는 미국에서 2세부터 17세 뇌전증 환자에게 처방이 가능해진다. 미국에서 2세~17세 뇌전증 환자 비중은 전체 환자 중 20~30% 수준으로 알려졌다.
SK바이오팜 관계자는 “엑스코프리의 미국 소아 임상 3상은 2024년 말 품목허가를 신청해 2025년 시판을 예상하고 있다”면서 “미국에서 허가받으면 해당 임상 결과가 유럽의약품청(EMA)에서도 그대로 통용될 것이다. 유럽에서도 환자군 확대에 따른 로열티 수익이 늘어날 수 있다”고 내다봤다. 이어 “일본, 중국 등에서 진행 중인 엑스코프리 아시아 임상 역시 2024년 완료, 2025년 출시 예정”이라고 덧붙였다.
엑스코프리는 현재 독일 등 유럽 8개국에 출시돼 있다. 엑스코프리의 유럽 출시 국가는 향후 40개국까지 순차 확대될 예정이다. SK바이오팜은 엑스코프리 유럽 판매에 따른 두자릿수 로열티를 받고 있다. 엑스코프리는 EMA 허가를 받을 때, 별도 임상 없이 미국 FDA 임상데이터를 그대로 인정받았다.
글로벌 뇌전증 시장규모는 지난 2018년 기준 61억달러(8조원)이고 이 중 미국 시장이 33억달러(4조3692억원)를 차지하고 있다. 미국 뇌전증 시장 규모는 오는 2024년까지 41억달러(5조4284억원) 규모로 성장할 전망이다.
한편, 엑스코프리는 국내 기업이 미국 FDA로부터 품목허가 승인을 받은 유일한 신약이다. 국내 제약바이오사가 미국 의료시장에서 처방 매출을 올리는 약은 엑스코프리뿐이다.


.png)
.png)