|
TPX-114·TPX-115, 각각 국내 임상 3상과 2상 완료 앞둬
TPX-114의 국내 임상 3상 환자 모니터링은 올해 2분기 내 완료될 예정이다. 한직현 테고사이언스 이사는 “현재 임상 종료 후 모니터링 중이다. 종료된 후 결과분석을 거쳐 임상 보고서를 작성한다. 품목허가 신청은 4분기로 예상한다”고 했다. 현재 독립적 평가자가 24주 시점에서 MRI 판독을 통해 재파열율로 효능을 평가하는 환자 모니터링이 진행되고 있다.
TPX-115 미국 임상 2상 신청도 올해 이뤄질 계획이다. 한 이사는 “현재 미국 임상을 위한 임상시험수탁기관(CRO)을 선정 중이다. 올 4분기 미국 FDA(식품의약국) 품목허가 신청을 예상한다”고 말했다.
TPX-115의 경우 국내 임상도 진행되고 있다. 현재 임상 2상 환자는 모두 등록이 끝났고 모니터링 진행 중이다. 회사에 따르면 모니터링은 1분기에 완료될 예정이다.
테고사이언스는 TPX-115의 미국 상용화를 우선 진행한 후, TPX-114 글로벌 임상도 실행을 염두에 두고 있다는 입장을 밝혔다. 한 이사는 “TPX-115는 이르면 2026년에 FDA 품목허가 신청을 예상한다. 전략적으로 TPX-115를 우선 개시한 후 TPX-114에 대한 해외 임상을 진행할 예정이다”고 했다.
회전근개 파열 치료제 시장 전망은 긍정적이다. 글로벌 시장조사업체 ‘Variant Market Research’에 따르면, 글로벌 회전근개 파열 치료제 시장은 2015년 약 7조원에서 2024년께 약 15조원 규모로 성장할 것으로 전망된다. BIS Research에 따르면, 글로벌 세포치료제 시장은 2018년 약 1조원에서 2025년에는 약 14조원으로 성장할 것으로 예측된다. 같은 기간 우리나라 세포치료제 시장은 약 777억원에서 약 8633억원으로 증가할 전망이다.
근본 치료제로 미충족 수요 공략…올해 매출액 전망치 110억원
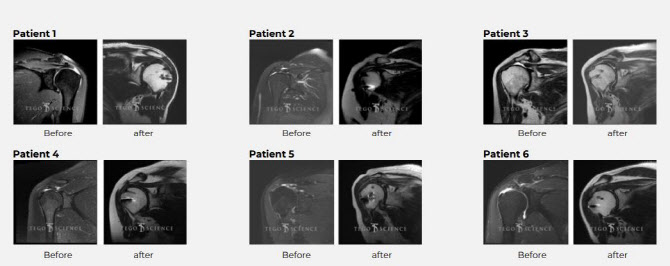
회사는 안전성과 효능을 바탕으로 시장 침투에 속도를 낸다는 계획이다. 회전근개 파열의 경우 힘줄을 재생시키는 근본 치료제는 없는 상황이다. 지난해 11월 미국 스포츠의학저널(Orthopedic Journal of Sports Medicine)에 게재된 TPX-114 임상 1상 결과에 따르면, TPX-114를 투여받은 회전근개전층파열 환자 6명 모두 부작용 없이 힘줄 재생이 촉진됐다. TPX-114는 자가유래 세포치료제라 용법과 용량을 탐색하는 2상이 생략됐다.
|
현재로선 TPX-114의 임상 단계가 좀 더 빠르지만, 시장성이 높은 TPX-115에 좀 더 집중한다는 게 회사 계획이다. 한직헌 이사는 “자기유래 세포치료제는 중증 환자가 대상이라 시장성에 한계가 있다. 동종유래 세포치료제는 그보다 경증 환자에 적용될 수 있어 수요가 많을 것”이라고 내다봤다.
그는 “올해는 당사에서 4, 5번째로 개발되는 자기·동종유래 세포치료제 임상 성공이 가장 중요한 목표다. TPX-115 미국 임상 2상이 성공하면, 3상 임상시험계획(IND)을 신청하는 데 전력을 다할 계획”이라고 밝혔다. 회사는 피부세포치료제 ‘홀로덤’과 ‘칼로덤’, 주름개선 세포치료제 ‘로스미스’ 등 3개 의약품을 개발해 판매 중이다.
한편 테고사이언스는 올해 매출액 전망치를 110억원으로 제시했다. 회사 관계자는 “지난해 매출은 80억원 내외가 될 것 같다. 지난해 1~3분기까지는 영업적자였지만, 4분기에는 흑자를 기록한 것으로 보고 있다. 지난해부터 세포치료제 위탁개발생산(CDMO)에서의 매출이 나오고 있고, 올해는 SK케미칼(285130)과 공동판매 계약을 맺은 칼로덤 매출이 활성화할 것으로 예상한다”고 밝혔다.
테고사이언스 2020년 매출액은 전년 대비 38.5% 증가한 87억8000만원, 영업이익은 355.4% 증가한 15억7500만원이었다. 2021년 1~3분기까지는 누적 매출 55억3433만원, 영업손실 12억2485만원을 기록했다.

.png)
.png)










![‘다주택자' 한성숙 장관, 모친 거주 송파구 아파트 처분[only이데일리]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26043001539t.jpg)
