|
LBC 과정 빠진 마이랩 CER…“부분 자동화 단계 수준”
노을의 마이랩 CER은 후단 중심 역량만 갖춘 상태로 전 과정 자동화 솔루션이라고 보긴 어려운 상태다. 노을의 자궁경부암 진단 솔루션에는 액상세포검사(LBC) 단계가 포함돼 있지 않다. 자궁경부암 진단 과정은 전처리(LBC)→염색→이미징→AI 분석의 과정을 거친다.
LBC 단계는 모든 진단의 기초 데이터 품질을 결정하는 관문이기 때문에 해당 단계가 빠지면 샘플 품질에 편차가 생기고, 판독 정확도가 떨어져 데이터 신뢰도에 문제가 생긴다. 자체 LBC 솔루션이 없으면 타사 제품에 의존해야 하는데 이 경우 원가 문제가 생기게 된다.
업계 관계자는 “자궁경부암 진단 솔루션이 뒷단에 있는 영상 판독 기술 위주만 갖추고 있다 보니 어디서 어떻게 검체 채취를 하고 슬라이드를 제공받을지가 문제”라며 “검체 준비부터 전처리가 중요한데 이런 앞단의 프로세스는 자체 솔루션이 없기 때문에 이 역할을 할 다른 업체와 손을 잡아야 할 것”이라고 짚었다.
이는 유럽 인허가 획득에도 걸림돌이 될 수 있다. 노을은 마이랩 디바이스와 말라리아, 혈구분석, 자궁경부암 진단 카트리지의 유럽 CE-IVDD 인증을 획득했다. CE-IVDD는 구(舊) 체외진단 규제 체계이기 때문에 2022년부터 시행 중인 CE-IVDR 인증을 획득해야 한다. 이 중 플랫폼인 마이랩 디바이스는 IVDR 요건에 따른 적합성 선언(DoC)을 진행했지만 카트리지들은 IVDR 인증을 획득해야 하는 상태다. 노을은 CE-IVDR 인증 획득을 위해 1억5000만원을 사용할 계획이다.
문제는 IVDR 체계에서는 시스템 단위 검증(System Validation)이 중요하다는 점이다. LBC가 외부 제품이면 전체 시스템으로서 성능·재현성 평가가 복잡해지는 측면이 있다. CE-IVDR 인증 획득이 지연되면 고수익이 기대되는 유럽 시장에서 점유율을 높이는 데 어려움을 겪을 수 있다.
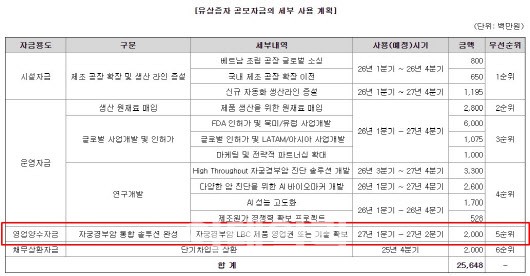
노을은 이 같은 문제점을 인식하고 LBC 제품의 영업권 또는 기술 확보를 위해 자금 조달에 나섰다. 이번에 350억원 규모의 주주배정 유상증자를 결정한 이유 중 하나도 LBC 기술 확보였다. 노을의 유증 공모자금 사용 계획에는 5순위로 LBC 영업권 또는 기술 확보에 20억원을 투자할 예정이라고 기재돼 있다.
|
마이랩 CER의 글로벌 경쟁력에 대해서도 의구심이 제기된다. 현재 노을의 자궁경부암 진단 솔루션은 일 평균 20~30건 내외의 진단이 가능하다. 이는 경쟁사들의 자동화 솔루션이 1일 170~200 슬라이드 처리가 가능한 것과 비교해 상당한 격차가 있다.
뿐만 아니라 대형 병원이나 대형 진단검사센터가 요구하는 수백건의 1일 처리량을 고려해도 경쟁력이 떨어진다는 평가다. 해외 주요 진단기관은 8시간에 150건 이상의 처리량을 요구하는 경우가 많다. 글로벌 시장 진출을 위해서는 처리량을 높일 필요가 있는 셈이다.
노을은 일 평균 100~200건 수준의 진단이 가능한 자궁경부암 진단 솔루션을 개발할 계획이다. 이를 위해 차세대 카메라·광학계, 인공지능(AI) 칩과 자동화 솔루션 등을 개발할 예정이다. 대용량 검사를 위한 신규 카트리지도 추가로 개발할 방침이다.
노을 관계자는 “글로벌 자궁경부암 시장 내 경쟁력을 강화하기 위해 차세대 고속 자궁경부암 진단 솔루션 개발을 구상·준비 중”이라며 “이를 통해 대용량 검사가 필요한 대형병원이나 대규모 진단랩의 수요에 대한 경쟁력을 향상시킬 수 있을 것”이라고 말했다.


.png)
.png)