|
미국에서 출발한 네오이뮨텍, 2021년 코스닥서 상장
네오이뮨텍은 2014년 미국 메릴랜드주 록빌에서 출발한 기업이다. 이 지역에는 미국국립보건원(NIH)과 미국 식품의약국(FDA)등이 위치한다. 설립자인 양세환 대표는 2001년 포항공대 박사학위를 받았다. 이어 2006년까지 같은 곳에서 박사후연구원으로 단백질 성능 개발 연구를 수행했다. 그는 이때 단백질의 수명을 늘리는 ‘하이브리드FC(hyFc)’ 융합 기술 등을 개발해 제넥신(095700)에 참여했고, 연구소장으로 약 7년을 근무했다.
양 대표는 “신약 후보물질 개발부터 일본이나 중국 등 해외 기술이전까지 제넥신에서 다양한 업무를 경험했다”며 “글로벌 의약품 시장을 주름잡는 미국에서 신약 개발을 진행해야 한다는 생각이 들기 시작했고, 네오이뮨텍을 미국에 설립하게 됐다”고 설명했다.
그가 네오이뮨텍을 설립한 해에 FDA는 미국 머크의 ‘키트루다(성분명 펨브롤리주맙)’나 브리스톨마이어스스큅(BMS)의 ‘옵디보(성분명 니볼루맙)’ 등과 같은 3세대 면역항암제에 대한 판매 승인을 내리고 있었다. 양 대표는 “2010년대 들어 화제가 된 면역항암제 관련 논문을 무수히 봤다”며 “제넥신에서 직접 개발 중이던 신약 후보물질 중 하나가 면역항암제로 작용할 수 있다는 생각이 들었다. 그 물질이 현재 우리의 주력 무기인 ‘NT-I7(성분명 에피넵타킨 알파)’다”고 덧붙였다.
체내 신호전달 물질인 ‘인터류킨(IL)-7’은 면역세포인 T세포의 수를 늘리는 기능을 갖고 있어 T세포 증폭제로 불린다. 하지만 그 기능이 유지되는 반감기가 수시간 이하로 짧다. NT-I7은 네오이뮨텍이 보유한 특허 기술을 이용해 IL-7의 반감기와 산업적인 생산 수율을 크게 증가시킨 신약 후보물질이다.
양 대표는 “2015년 이후부터 NT-I7로 투자를 유치했고, 이후 글로벌 제약사(빅파마)들과 임상 프로젝트 계약을 속속 체결하기 시작했다”며 “이 기술력과 실적을 인정받아 2021년 국내 코스닥에 상장했다”고 말했다.
가장 앞선 T세포 증폭제 개발 기업...임상 결과 속속 청신호
미국과 유럽 등에서 T세포 증폭제 관련 신약 후보물질로 임상 단계의 연구개발을 진행 중인 기업은 네오이뮨텍뿐이다.
사실 IL-7에 주목한 첫 기업은 프랑스 제약사 사이더리스(Cytheris)였다. 사이더리스는 2000년대 중후반 자체개발한 IL-7 관련 물질로 후천성면역결핍증후군(AIDS, 에이즈)이나 B형 감염 등에 적용하기 위한 임상을 시도한 바 있다. 회사 측은 이 물질로 바이러스를 공격할 T세포가 늘어나는 효과를 확인했다.
양 대표는 “우리가 생산한 NT-I7은 사이더리스의 물질보다 반감기는 10배, 생산 수율은 100배 이상 우수하며, 암을 공격하는데 특이적인 T세포 생산에 최적화된 상태다”고 설명했다. 이어 “추가 특허를 내면서 우리 물질에 대한 방호벽을 쌓아가고 있다”고 말했다.
그에 따르면 코로나19 백신처럼 T세포 증폭제를 메신저리보핵산(mRNA)의 형태로 넣어주는 기업이나 IL-7과 다른 항암 물질을 이중항체로 구성한 약물을 설계하는 기업 등이 여러 지역에 존재한다. 양 대표는 “여러 기업이 T세포 증폭제를 활용해 신약 개발을 시도하기 시작했지만, 미국과 유럽을 통틀어 우리만 유일하게 임상 단계에 진입한 상태다”고 강조했다.
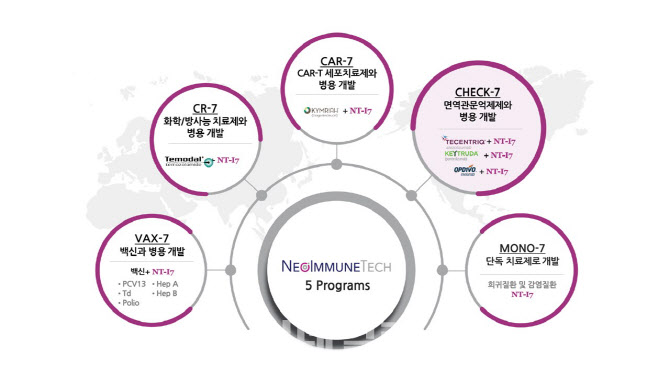
NT-I7은 현재 항암(10건)과 코로나19 등 감염 질환(4건), 급성방사선 증후군 등 기타 질환(1건) 등 총 15건에 임상 프로젝트를 진행 중이다. 여기에는 스위스 로슈 ‘티쎈트릭(성분명 아테졸리주맙)’, 머크의 키트루다, BMS의 옵디보 등 빅파마와 계약을 맺고 함께 수행하는 병용임상 연구 4건도 포함된다.
회사 측은 지난해 11월 미국 워싱텅DC에서 진행한 면역항암학회(SITC)에서 키트루다와 NT-I7을 병용투여하는 임상 2a상 중간결과를 발표했다. 키트루다 단독요법 시 효과가 전혀 없었던 일부 난치성 암에서 NT-I7 병용요법을 쓰면 효과를 발휘한다는 내용이었다. 양 대표는 “빅파마들과 하는 임상은 이미 임상 1/2상 또는 2상인 상태”라며 “이들의 약물을 단독으로 사용하는 것보다 NT-I7을 함께 쓸 때 효과가 더 크다는 연구 결과가 다양하게 축적되고 있다”고 말했다.
|
신약개발 원년 2.0 선포...“기술이전, 가속승인 등 개발 속도 낼 것”
네오이뮨텍은 자체적으로 올해를 ‘신약개발 원년 2.0’으로 선포했다. 양 대표는 “설립 후부터 2021년까지 NT-I7의 임상 파트너를 찾아 연구를 축적한 ‘1.0’시기였다”며 “올해부터는 기술이전과 품목허가를 최우선 목표로 뛰는 ‘2.0’시기로 판단하고 있다”고 강조했다.
이를 위해 네오이뮨텍은 지금까지 진행된 NT-I7의 임상 결과를 바탕으로 FDA로부터 주요 적응증에 대한 가속승인을 받을 수 있도록 만드는 전략 수립 작업에 착수한 상태다. 양 대표는 “빅파마의 면역항암제와 NT-I7의 병용임상이나 우리 물질의 단독임상 등에서 강력한 효과가 입증되고 있는 만큼 미국에서 기술이전 또는 가속 승인 등 최적화된 신약 개발 성과를 이뤄낼 수 있도록 노력할 것”이라고 말했다.

.png)
.png)